Retirada preventiva de útero, trompas e ovários em mulheres com Síndrome de Lynch
 São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
Estudo publicado na revista Nature discute benefícios da cirurgia profilática; indicação deve ocorrer apenas quando pacientes já formaram a prole conforme desejo pessoal
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
Sem dúvida, desde 2011, quando a atriz Angelina Jolie anunciou a realização da cirurgia profilática para retirada dos
ovários e das trompas de Falópio, depois de já ter feito uma dupla mastectomia, houve um grande entendimento popular
sobre o que são as mutações hereditárias do câncer, em especial do gene BRCA1, relacionado ao caso da atriz, e BRCA2,
cujas mutações também têm grande impacto na predisposição aos cânceres femininos. Contudo, cerca de dez anos depois, a
discussão precisa ser ampliada para as outras síndromes hereditárias causadoras de tumores em mulheres, a exemplo da
síndrome de Lynch.
Direito à mamografia de rastreamento no Brasil
 São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
Discussão sobre qual a idade ideal para iniciar a realização dos exames de mamografia ainda divide opiniões; personalização da indicação é a resposta.
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
Não é novidade que a mamografia é atualmente o melhor método de base populacional para detecção precoce do câncer de
mama, quando as chances de sucesso do tratamento são maiores. Chamando atenção sobre isso, na última semana, recebi um
e-mail da diretora médica da Pfizer Brasil, Dra. Márjori Dulcine, a respeito da campanha Mamografia no SUS a partir dos
40 anos, cujo objetivo é engajar a sociedade brasileira a buscar a aprovação do Projeto de Decreto Legislativo 679/2019,
que assegura o direito à realização da Mmamografia preventiva no SUS para mulheres a partir dos 40 anos.
Qual o peso do álcool na incidência e mortalidade por câncer nos EUA?
 São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
Assim como ocorre no tabagismo, o combate a esse hábito, com implementação de protocolos mundiais, políticas federais e estaduais, mostra-se como ferramenta eficaz contra câncer
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
O tema álcool é recorrente quando falamos do combate ao câncer devido a sua influência direta no processo de
carcinogênese. Tumores de boca, faringe, laringe, esôfago, estômago, fígado, intestino (cólon e reto) e mama, além de
pelo menos outras 200 doenças e lesões são comuns de aparecer em pessoas com hábitos alcoólicos.
Dia Mundial do Câncer: ações anticâncer precisam ser diárias
 São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
São necessárias ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde
Os 10 tipos de câncer mais comuns em 2020 são responsáveis por mais de 60% dos casos de câncer recém-diagnosticados e mais de 70% das mortes pela doença; prevenção envolve hábitos de vida saudáveis.
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
Nesta quinta-feira (4/2), temos o Dia Mundial do Câncer, data dedicada a chamar a atenção sobre a necessidade diária de ações preventivas contra o câncer, tanto por parte da população, como das autoridades governamentais e instituições de saúde.
Taxas de câncer crescem entre adolescentes e jovens adultos dos EUA

Melhor compreensão dos tipos de tumores crescentes nesse grupo permitirá aperfeiçoar protocolos de prevenção,
rastreamento, diagnóstico e tratamento específicos
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
Via de regra, excetuando-se os casos hereditários, consideramos o câncer uma doença do envelhecimento, pois o processo
de carcinogênese ocorre em longo prazo. Dessa forma, a maior parte dos protocolos indicam exames de rastreamento em
torno dos 50, 55 anos. Contudo, os hábitos de vida da humanidade parecem estar mudando essa regra, sendo registrados
tumores em pessoas cada vez mais jovens.
Protetor solar é ferramenta eficaz para prevenção do melanoma

Estudo de custo-efetividade realizado entre a população australiana comparou prevenção versus detecção precoce para o
controle de longo prazo de melanoma
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
O melanoma é o tipo de câncer de pele que mais mata, apesar de corresponder a apenas 1% dos casos que atingem
esse
órgão. A cada ano do triênio 2020/2022 deverão ser diagnosticados no Brasil 8.450 novos casos de câncer de pele tipo
melanoma (4.200 em homens e 4.250 em mulheres), conforme dados do Instituto Nacional de Câncer – INCA.
Como funcionam as vacinas de RNA mensageiro (mRNA) para a prevenção
da covid-19
 -->
-->
Com confirmação de eficácia em mais de 95%, governos de vários países já negociam compra de lotes
dessas vacina
Com o avanço das pesquisas que comprovam a eficácia de algumas das vacinas contra Covid-19 e o
início das negociações para a aquisição dessas vacinas, muito tem se falado sobre o tema. São duas
as vacinas de mRNA, uma desenvolvida pela farmacêutica Moderna, dos EUA, com 94,5% de eficácia; e a
outra pela também norte-americana Pfizer, em parceria com a empresa alemã de biotecnologia BioNTech,
com capacidade de imunização de até 95%. Confira agora os esclarecimentos do nosso diretor executivo
Dr. André Murad, que é Médico Oncologista Pós-Doutor em Genética, sobre o que é e como funciona uma
vacina de mRNA.
Atraso no tratamento do câncer aumenta risco de morte em até 13% a
cada mês
Estudos iniciados para a melhor compreensão do impacto do atraso do tratamento durante a pandemia
servem de alerta
sobre a necessidade de otimização dos sistemas globais de saúde
André Murad - Oncologista, diretor Executivo da Personal Oncologia de Precisão e
Personalizada e
Oncogeneticista no Centro de Câncer Brasília / Cettro
Desde o início da quarentena, quando percebi que pacientes começaram a desmarcar consultas e
que os novos pacientes
pararam de chegar para que fossem diagnosticados, tenho alertado sobre as consequências futuras da
interrupção de
tratamentos e do aumento dos diagnósticos tardios. Não demorou muito para que as inúmeras
entidades médicas responsáveis
divulgassem dados preocupantes.
OUTUBRO ROSA: SÉRIE DE LIVES LEVARÁ INFORMAÇÕES DIRETAMENTE PARA A
CASA DAS MULHERES

Para especialistas, crescimento do diagnóstico tardio, em 2020, repercutirá em maiores taxas de
mortalidade por câncer de mama
Em tempos de pandemia, as ações do Outubro Rosa para a conscientização do câncer de mama serão
apresentadas no formato
preferido do momento: lives no Instagram. Na Personal Oncologia de Precisão, sete palestras serão
realizadas ao vivo
pela rede social, ao longo do mês, com a participação de especialistas em oncologia, mastologia e de
mulheres que
passaram pelo tratamento.
Combate à obesidade é ferramenta fundamental contra Câncer
Ginecológico
 Independentemente da massa corpórea, mulheres e homens ativos fisicamente apresentam risco mais
baixo de desenvolver alguns dos tipos mais prevalentes de câncer
Independentemente da massa corpórea, mulheres e homens ativos fisicamente apresentam risco mais
baixo de desenvolver alguns dos tipos mais prevalentes de câncer
Mês de conscientização: Descontrole hormonal, processo inflamatório crônico e erro alimentar
justificam obesidade como causa do câncer
Dr. André Murad – Oncologista, diretor Executivo da Personal Oncologia de Precisão e
Personalizada e Oncogeneticista no Centro de Câncer Brasília - Cettro
Setembro é também o mês de conscientização do Câncer Ginecológico, que inclui câncer do colo de
útero e de ovário, além
dos tumores de endométrio, vagina e vulva. Meu alerta nesta semana é, sobretudo, a respeito da
obesidade e sedentarismo
como fatores de risco para o desenvolvimento destes e de outros tipos de tumores. Trata-se do
segundo principal fator de
risco para o desenvolvimento de câncer, atrás apenas do tabagismo, de acordo a Organização Mundial
de Saúde (OMS).
Avanços no tratamento do câncer colorretal são
promissores
 Identificação de mutações e biomarcadores moleculares possibilitam utilização de terapias-alvo e
de imunoterapia
Identificação de mutações e biomarcadores moleculares possibilitam utilização de terapias-alvo e
de imunoterapia
Detecção de novos alvos terapêuticos por meio da Biópsia Líquida ampliam estratégias terapêuticas
para pacientes com tumores avançados
Dr. André Murad – Oncologista, diretor Executivo da Personal Oncologia de Precisão e
Personalizada e Oncogeneticista no Centro de Câncer Brasília - Cettro
Conforme eu disse em minha última coluna, aqui no Saúde Plena, em virtude do Setembro Verde - mês
dedicado à prevenção
do câncer colorretal, nesta semana abordarei uma boa notícia: os consideráveis avanços obtidos no
tratamento do câncer
colorretal metastático nas duas últimas décadas. Primeiramente, a quimioterapia ganhou novos regimes
à base de
oxaliplatina e Irinotecano, que foram incorporados à já tradicional combinação de uma fluopirimidina
(5-fluorouracil ou
capecitabina) e leucovorina.
Setembro Verde: mês da conscientização sobre o Câncer
Colorretal
 O talentoso ator norte-americano Chadwick Boseman foi uma das vítimas jovens de câncer
colorretal
O talentoso ator norte-americano Chadwick Boseman foi uma das vítimas jovens de câncer
colorretal
Alerta: incidência de câncer colorretal está aumentando em pessoas mais jovens e hábitos de vida
podem ser as principais causas
Dr. André Murad – Oncologista, diretor Executivo da Personal Oncologia de Precisão e
Personalizada e Oncogeneticista no Centro de Câncer Brasília - Cettro
O talentoso ator norte-americano Chadwick Boseman morreu de câncer colorretal (CCR) (também chamado
cólon e reto) com
apenas 43 anos de idade e o fato chamou a atenção para este fenômeno, já tão bem documentado pela
ciência: as taxas de
incidência e mortalidade associadas ao CCR nos Estados Unidos têm diminuído nas últimas décadas, em
grande parte devido
ao aumento da captação do rastreamento do CCR. Mas, infelizmente, a tendência oposta foi observada
entre pacientes com
menos de idade 50 anos.
Promessa virando realidade: Biópsia líquida pode detectar câncer anos
antes de sintomas aparecerem
 Biópsia líquida é uma tecnologia não invasiva capaz de detectar biomarcadores moleculares por
meio de uma coleta simples de sangue
Biópsia líquida é uma tecnologia não invasiva capaz de detectar biomarcadores moleculares por
meio de uma coleta simples de sangue
Exame possui tecnologia não invasiva para a detecção de biomarcadores moleculares por meio de uma
coleta simples de sangue
Dr. André Murad – Oncologista, diretor Executivo da Personal Oncologia de Precisão e
Personalizada e Oncogeneticista no Centro de Câncer Brasília - Cettro
Todos nós sabemos da importância do diagnóstico precoce para o sucesso do tratamento do
câncer. Podemos afirmar que, em
fases iniciais e em uma elevada porcentagem dos casos, a grande maioria dos cânceres é curável. Mas,
o grande desafio
que enfrentamos é como detectá-lo precocemente. Via de regra, quando um câncer provoca
sintomas, ele já se encontra em
uma fase avançada de seu desenvolvimento.
A genômica e o desenvolvimento de vacinas para a Covid-19
 A função da vacina é “treinar” o nosso sistema imunológico para reconhecer e atacar o vírus
quando o encontrar.
A função da vacina é “treinar” o nosso sistema imunológico para reconhecer e atacar o vírus
quando o encontrar.
Existem mais de 100 projetos de desenvolvimento de vacinas para COVID-19 em todo o mundo; 8
vacinas já estão em testes clínicos em seres humanos
Dr. André Murad – Oncologista, diretor Executivo da Personal Oncologia de Precisão e
Personalizada e Oncogeneticista no Centro de Câncer Brasília - Cettro
Vivemos uma verdadeira corrida entre as principais potências mundiais, que buscam em tempo recorde
desenvolver uma
vacina eficaz contra o COVID-19. De forma geral, uma vacina é projetada para proteger as
pessoas antes de serem expostas
a um vírus - neste caso, o novo coronavírus SARS-CoV-2, cuja infecção já acometeu mais de 20
milhões de indivíduos em
todo o mundo e já matou mais de 700 mil pessoas, 100 mil somente no Brasil.
FDA aprovava primeira biópsia líquida para perfil abrangente de
mutação tumoral em todos os cânceres sólidos
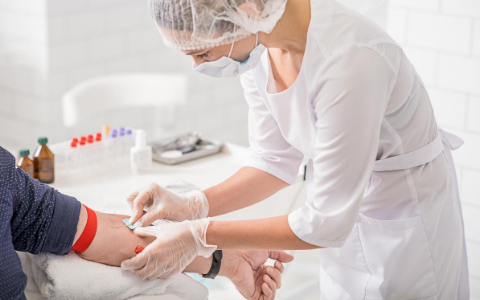 Aprovação do Guardant360 CDx demonstra ampliação e benefícios da biópsia líquida
Aprovação do Guardant360 CDx demonstra ampliação e benefícios da biópsia líquida
Guardant360 CDx fornece informações genômicas críticas para oncologistas a partir de uma simples
coleta de sangue
A Food and Drug Administration (FDA) dos EUA aprovou o Guardant360 ® CDx para perfil de mutação
tumoral, também
conhecido como perfil genômico abrangente (CGP), em pacientes com qualquer neoplasia maligna sólida
(tumor canceroso). O
Guardant360 CDx também foi aprovado como um diagnóstico complementar para identificar
pacientes com câncer de pulmão de
células não pequenas com alterações no receptor do fator de crescimento epidérmico (EGFR ) que podem
se beneficiar do
tratamento com Tagrisso ® (osimertinibe). O Guardant360 CDx oferece aos pacientes e médicos um
exame de sangue simples e
rápido para ajudar a informar as opções de tratamento personalizadas.
Rastreio do câncer do colo uterino tem novas diretrizes;
conheça
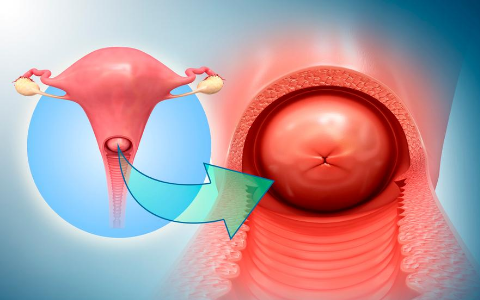
Nova diretriz da Sociedade Americana do Câncer exige menos e mais simplificado rastreamento do
câncer cervical
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e
Personalizada
Diante de um novo cenário de registro de câncer de colo de útero, também chamado cervical, a
American Cancer Society -
Sociedade Americana do Câncer atualizou e simplificou as recomendações para rastreamento da doença
nos EUA.
Desafios da Oncologia de Precisão
 Os termos oncogenética e oncogenômica não são ainda muito difundidos na comunidade na médica,
muito menos entre a população
Os termos oncogenética e oncogenômica não são ainda muito difundidos na comunidade na médica,
muito menos entre a população
Genética e Genômica vêm revolucionando a prevenção, o diagnóstico e o tratamento do câncer, mas
pouca difusão desses
conhecimentos ainda impede ampla aplicação clínica
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e
Personalizada
As chamadas terapias-alvo e os conhecimentos sobre genética aplicáveis à prevenção, rastreamento e
tratamento oncológico
compõem hoje a pedra angular da oncologia moderna, a chamada de oncologia de precisão. Todavia, os
termos oncogenética e
oncogenômica não são ainda muito difundidos na comunidade na médica, muito menos entre a
população.
Entenda como a genética individual influencia a gravidade e o
prognóstico da COVID-19
 Variações genéticas podem resultar em proteínas mais ou menos eficazes no reconhecimento e na
sinalização da presença do coronavírus no corpo
Variações genéticas podem resultar em proteínas mais ou menos eficazes no reconhecimento e na
sinalização da presença do coronavírus no corpo
Estudos preliminares apontam que as características genéticas podem ser responsáveis por reações
tão diferentes entre os infectados pelo SARS-CoV-2
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Quem me acompanha aqui sabe que sou um completo apaixonado pelo que o entendimento da genética
oferece de possibilidades
de prevenção e combate a inúmeras doenças. E não poderia ser diferente em relação ao
SARS-CoV-2 (sigla do inglês, Severe
Acute Respiratory Syndrome Coronavirus 2). Perguntas como “o que faz com que uma pessoa jovem e
saudável contraia o novo
coronavírus e acabe lutando pela vida em ventilação mecânica, enquanto outra tem infecção
praticamente assintomática?”
têm sido objetivo de curiosidade de muitas pessoas.
Efeito preventivo da aspirina para câncer colorretal causado pela
Síndrome de Lynch
 Diagnóstico da Síndrome de Lynch em um indivíduo antes do aparecimento de um tumor aparecer pode
mudar a vida de toda a família
Diagnóstico da Síndrome de Lynch em um indivíduo antes do aparecimento de um tumor aparecer pode
mudar a vida de toda a família
Após as análises das evidências acumuladas em mais de 20 anos, pesquisadores concluíram que o
uso preventivo de aspirina reduz o risco deste câncer
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
As Síndromes de Predisposição Hereditária ao Câncer são responsáveis por entre 10 e 15% dos
casos de câncer no mundo e,
por isso, algumas pessoas não dão muita atenção ao diagnóstico destas. Mas, a lógica é outra. As
mutações hereditárias
são justamente aquelas que podemos prever de forma objetiva, possibilitando uma atuação assertiva e
preventiva do câncer
em seus portadores.
Cirurgião Oncológico – Atuação preventiva é cada vez mais
comum
 Cirurgiões Oncológicos têm atuação primordial no diagnóstico, prognóstico, assim como na retirada
muitas vezes complexas de tumores
Cirurgiões Oncológicos têm atuação primordial no diagnóstico, prognóstico, assim como na retirada
muitas vezes complexas de tumores
Com os avanços da oncogenética, cirurgias profiláticas ou redutoras de risco se tornaram
ferramenta de combate ao câncer
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
A última sexta-feira, dia 17, foi dedicada aos cirurgiões oncológicos, especialidade da
medicina que, tradicionalmente,
dedica-se à realização de cirurgias em pacientes oncológicos. Esses profissionais têm atuação
primordial no diagnóstico,
prognóstico, assim como na retirada muitas vezes complexas de tumores e realização de tratamentos
cirúrgicos paliativos.
Então, primeiramente registro meu agradecimento a todos os colegas que se dedicam a essa nobre e
complexa tarefa.
Sociedade Americana de Câncer atualiza diretrizes para prevenção do
câncer
 Pelo menos 18% de todos os casos de câncer nos Estados Unidos estão relacionados à combinação de
fatores de hábitos de vida
Pelo menos 18% de todos os casos de câncer nos Estados Unidos estão relacionados à combinação de
fatores de hábitos de vida
Manter um peso saudável, permanecer ativo durante toda a vida, seguir um padrão de alimentação
saudável e evitar ou
limitar o álcool são algumas das recomendações
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Quem acompanha minha coluna aqui no Saúde Plena, ou já assistiu a uma de minhas palestras,
deve saber que sou enfático
sobre a importância da prevenção do câncer por meio do controle dos fatores de risco, sejam
eles hereditários – testes
genéticos detectam as Síndromes de Predisposição Hereditária permitindo uma prevenção personalizada
–, sejam
relacionados à adoção de hábitos de vida saudáveis. Além de minha experiência clínica
demonstrar que a prevenção é
sempre o melhor caminho, as pesquisas comprovam que praticamente metade dos casos de câncer são
evitáveis.
Direitos dos pacientes oncológicos
 Em MG, a Lei 23.449/2019 garante às mulheres, com alto risco de desenvolvimento de câncer de mama
e de ovário, a realização de testes genéticos
Em MG, a Lei 23.449/2019 garante às mulheres, com alto risco de desenvolvimento de câncer de mama
e de ovário, a realização de testes genéticos
Embora a Constituição assegure o direito à saúde, algumas das tecnologias mais modernas, como
exames genéticos
preventivos, ainda não possuem cobertura do sistema público de saúde e sequer da rede
privada.
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Um dos principais motivos de aflição para os pacientes oncológicos ao receberem o diagnóstico
é não saber se poderão
custear as despesas do tratamento e como esse processo irá afetar compromissos como o
trabalho. Ocorre que o paciente
encontra guarida na Constituição da República Federativa do Brasil, que estabelece garantias
fundamentais a todo
cidadão, propiciando aos indivíduos condições mínimas para o pleno gozo de seus direitos,
sendo que, a saúde é
considerada um direito de todos e dever do Estado, com acesso universal e igualitário.
Estou com câncer, e agora?
 Atualmente, pacientes têm à disposição as chamadas terapias personalizadas e de precisão, que
podem ser utilizadas após a análise do perfil genético do tumor
Atualmente, pacientes têm à disposição as chamadas terapias personalizadas e de precisão, que
podem ser utilizadas após a análise do perfil genético do tumor
Entenda quais são as fases de enfrentamento do câncer, do diagnóstico ao tratamento, e por que
um atendimento
integrativo e multidisciplinar é um facilitador para o paciente oncológico
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
O processo de enfrentamento e de tratamento para combater o desenvolvimento do câncer
é desgastante e cansativo por
diferentes motivos, para o paciente e para seus familiares. Insegurança, medo e muitas dúvidas são
comuns desde os
primeiros momentos em que se pensa na possibilidade de se ter a doença.
O câncer de pulmão pode ser hereditário?
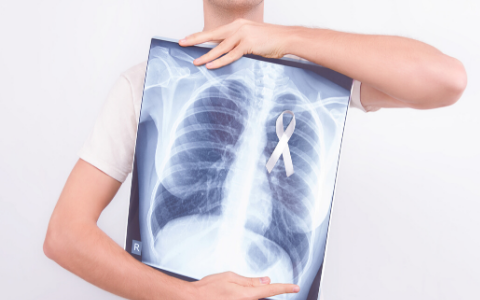 Variante genética encontrada pelos pesquisadores pode ajudar a identificar determinadas
populações com maior risco de câncer de pulmão
Variante genética encontrada pelos pesquisadores pode ajudar a identificar determinadas
populações com maior risco de câncer de pulmão
A incógnita do surgimento desses tumores em pessoas que não foram expostas a fatores de risco
como tabagismo e gás
radônio pode ter sido resolvida em estudo recente
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Casos familiares de câncer de pulmão sempre intrigaram aos médicos, especialmente a nós
oncogeneticistas. Não é incomum
identificarmos mais de um caso de câncer de pulmão em parentes de uma mesma família, em geral, em
idade abaixo dos 55
anos e, para os quais, as causas mais comuns de câncer de pulmão – o tabagismo ativo e
passivo – não podem ser
identificadas. Nesses casos, a predominância é de ocorrência em mulheres e o tipo tumoral mais
comumente descrito é o
adenocarcinoma.
Conheça a síndrome de predisposição ao câncer que chegou ao Brasil
junto com os tropeiros
 Pessoas com síndrome de Li-fraumeni podem apresentar até 50% de chance de desenvolver tumores
antes dos 30 anos de idade
Pessoas com síndrome de Li-fraumeni podem apresentar até 50% de chance de desenvolver tumores
antes dos 30 anos de idade
Portadores de mutações no gene TP53 (Síndrome de Li-Fraumeni) têm risco aumentado de desenvolver
tumores em múltiplos locais e são mais sensíveis à radiação ionizante
Algumas pessoas, mesmo tendo uma vida completamente saudável, acabam por desenvolver algum
tumor. “Coisa do destino?” Na
verdade, a ciência já mostrou que algumas pessoas nascem com determinadas mutações, que podem
predispor esses indivíduos
ao desenvolvimento de tumores: são as chamadas Síndromes Hereditárias de Predisposição ao
Câncer..
Pessoas com diversas mutações do gene TP53 como a mutação p.R337H, que é uma das variantes possíveis
neste gene, por
exemplo, têm risco aumentado de desenvolver tumores benignos e malignos em múltiplos locais, o que
caracteriza a chamada
Síndrome de Li-Fraumeni.
Na Europa, medicamentos para reposição hormonal devem informar sobre
risco aumentado de câncer de mama
 Uso da terapia de reposição por 10 anos resultou em cerca do dobro do risco de câncer de mama
Uso da terapia de reposição por 10 anos resultou em cerca do dobro do risco de câncer de mama
Estudos demonstram que, mesmo após a interrupção no uso da terapia, o risco poderia persistir
por até uma década, variando conforme a duração do uso
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
É uma premissa da ciência estar sempre em processo de atualização com a descoberta de novas
informações e a revisão do
que já se sabe. Essas análises, na maior parte das vezes, resultam em mudanças na prática da
medicina. Recentemente, por
exemplo, o Comitê de Avaliação de Risco de Farmacovigilância (PRAC), da Agência Europeia de Medicina
(EMA), recomendou a
atualização das informações de segurança de medicamentos para terapia de reposição hormonal
(TRH), após estudos de
revisão demonstrarem o risco associado de câncer de mama.
Câncer de mama masculino: desafios e promessas da Genética para
diagnóstico mais precoce e tratamento personalizado
 Em geral, os homens não têm conhecimento sobre o câncer de mama masculino e podem ignorar ou
sentirem-se desconfortáveis ao procurar atendimento
Em geral, os homens não têm conhecimento sobre o câncer de mama masculino e podem ignorar ou
sentirem-se desconfortáveis ao procurar atendimento
Mutações no gene BRCA2 representam o fator de risco mais forte para o câncer de mama masculino,
com um risco relativo de 80 vezes o da população em geral
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Todos os anos, temos campanhas oportunas para conscientizar às mulheres sobre a importância de
prevenção e rastreamento
dos cânceres de mama, ovário e útero; e para homens, sobre a prevenção do câncer de próstata.
Contudo, nem sempre há
espaço para falar sobre o câncer de mama masculino, cuja incidência está aumentando. Embora ainda
seja uma doença rara e
pouco compreendida, estudos genéticos recentes revelaram diferenças fundamentais em relação ao
câncer de mama feminino
que podem ajudar a orientar as estratégias de tratamento em direção a uma abordagem mais
personalizada.
Quais as novidades da Ciência sobre a interação obesidade e
câncer?
 Na última década, a obesidade tem sido associada a um aumento do risco e da agressividade de
vários tipos de câncer.
Na última década, a obesidade tem sido associada a um aumento do risco e da agressividade de
vários tipos de câncer.
Estudos recentes sobre o efeito biológico do tecido adiposo no desenvolvimento do câncer têm nos
auxiliado no entendimento desta relação
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Vários estudos epidemiológicos correlacionam a obesidade ao aparecimento de câncer. Um estudo
mais recente da União
Internacional de Controle do Câncer comprovou a relação entre obesidade e câncer. Ele estima
que 30% dos casos da
doença, nos países ocidentais, estejam relacionados ao sedentarismo e ao excesso de peso. Este é o
segundo fator de
risco para o desenvolvimento de câncer, ficando atrás apenas do tabagismo, de acordo a
Organização Mundial de Saúde
(OMS).
Entenda o papel das pesquisas clínicas no desenvolvimento de novos
medicamentos oncológicos
 Centros de pesquisas são oportunidade terapêutica extra para muitos pacientes
Centros de pesquisas são oportunidade terapêutica extra para muitos pacientes
O estado de Minas Gerais está inserido em uma extensa rede nacional e internacional de grupos de
pesquisa para análise de drogas que estarão disponíveis clinicamente em um futuro
próximo
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Talvez o câncer seja uma das doenças que há mais tempo acompanham a humanidade, embora
nem sempre tenha recebido tamanha
atenção como hoje. Cerca de 30 séculos antes de Cristo, os povos egípcios, persas e indianos já se
referiam à "doença de
tumores malignos". Desde a definição dos primeiros tratamentos – inicialmente,
cirúrgicos, depois com radioterapia,
seguido da quimioterapia – foram centenas de anos até a medicina oncológica chegar aos atuais
conceitos de oncologia de
precisão ou personalizada.
Infecção intermitente pode ser sinal premonitório de
câncer
 Pacientes podem experimentar uma maior ocorrência de infecções nos anos que antecedem o
diagnóstico de câncer
Pacientes podem experimentar uma maior ocorrência de infecções nos anos que antecedem o
diagnóstico de câncer
Um estudo japonês identificou que pacientes oncológicos tiveram taxas anuais de prevalência de
influenza,
gastroenterite, hepatite e pneumonia superiores nos anos antecedentes ao diagnóstico de
câncer
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Sabe-se que o câncer pode se desenvolver em um ambiente inflamatório causado por
infecções, interrupção da imunidade,
exposição a agentes cancerígenos químicos ou condições crônicas ou genéticas. Agora, um estudo
inovador realizado pelos
pesquisadores japoneses Shinako Inaida e Shigeo Matsuno – publicado na conceituada Cancer Immunology Research – mostrou
que pacientes podem experimentar uma maior ocorrência de infecções nos anos que antecedem o
diagnóstico de câncer.
Pacientes podem experimentar uma maior ocorrência de infecções nos
anos que antecedem o diagnóstico de câncer
 Diagnóstico da Síndrome de Lynch é confirmado com testes genéticos que realizam o sequenciamento
germinativo de todos os genes associados à condição
Diagnóstico da Síndrome de Lynch é confirmado com testes genéticos que realizam o sequenciamento
germinativo de todos os genes associados à condição
Adoecimento de vários membros familiares por câncer, antes dos 50 anos, é o principal critério
que leva médicos a suspeitarem da síndrome
Você conhece alguém que perdeu vários familiares devido ao câncer colorretal (cólon e reto ou de
intestino como
normalmente é conhecido)? Essa triste realidade acontece em algumas famílias e vários membros
jovens, a partir dos 35
anos, adoecem desse câncer ou até de tipos diferentes como ovário, endométrio,
pâncreas, estômago etc. Normalmente,
esses casos estão relacionados à chamada Síndrome de Lynch, que é um dos tipos de Síndrome
de Predisposição Hereditária
ao Câncer.
Inteligência artificial é hoje aliada no combate a
doenças
 Conhecimentos de IA possibilitaram aos pesquisadores da oncologia darem um salto no
desenvolvimento de soluções para diagnóstico precoce, prevenção e tratamento
Conhecimentos de IA possibilitaram aos pesquisadores da oncologia darem um salto no
desenvolvimento de soluções para diagnóstico precoce, prevenção e tratamento
Soluções de IA já são utilizadas na prática em áreas como a oncologia e vêm mostrando, agora,
grande importância em meio à pandemia de Covid-19
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Nos anos 1990, quando o cinema tratava de Inteligência Artificial (IA), apresentava distopias
em que essas tecnologias
eram aplicadas de formas mirabolante e inacreditável. Mas, na realidade, hoje, muitas vezes a IA
está presente na rotina
das pessoas de modo tão prático, que passa até despercebida. É importante pontuar esses avanços para
que a sociedade
continue apoiando investimentos e a continuidade dos estudos e pesquisas da área.
ANS orienta sobre a importância dos tratamentos continuados para garantir a saúde de pacientes
portadores de doenças comuns
.png) Tratamentos continuados, como diagnóstico e terapias em oncologia, não podem ser interrompidos,
sob pena de
colocarem em risco a vida dos pacientes
Tratamentos continuados, como diagnóstico e terapias em oncologia, não podem ser interrompidos,
sob pena de
colocarem em risco a vida dos pacientes
Diagnóstico e terapias em oncologia estão entre as especialidades citadas; entidade orientou
também sobre
atendimentos de urgência e emergência e sobre a realização das Internações e cirurgias
eletivas
Após o Governo Federal ter sancionado no dia 15 de abril a lei lei Nº
13.989, que autoriza o uso da telemedicina durante
a pandemia de coronavírus, a Agência Nacional de Saúde – ANS publicou também nota se pronunciando
sobre a
importância de
os cuidados com a saúde do brasileiro terem andamento durante a quarentena.
O FDA - Food and Drug Administration (órgão americano para aprovação, liberação e fiscalização de
medicamentos e
alimentos naquele país) aprovou o medicamento BRAFTOVI ® (encorafenib) em combinação com o
cetuximabe
(comercializado
como ERBITUX ®), para o tratamento de pacientes adultos com câncer colorretal metastático
portadores da
mutação BRAF
V600E, já tratados com terapias prévias.
Estudo com participação do Centro de Pesquisas Personal Oncologia tem
medicação aprovada pelo FDA para câncer colorretal
 Câncer colorretal é o terceiro tipo mais comum de câncer em homens e o segundo mais comum em
mulheres em todo o mundo
Câncer colorretal é o terceiro tipo mais comum de câncer em homens e o segundo mais comum em
mulheres em todo o mundo
Resultados mostraram que as drogas administradas melhoraram significativamente a sobrevivência
geral e alcançaram uma resposta superior ao tratamento padrão
Imagine poder diagnosticar o câncer precocemente por meio de uma simples coleta de sangue...A
realização dessa
possibilidade seria um grande avanço para a oncologia resultando em celeridade para o
tratamento, em mais qualidade de
vida e num processo menos dolorido e penoso para o paciente oncológico.
O FDA - Food and Drug Administration (órgão americano para aprovação, liberação e fiscalização de
medicamentos e
alimentos naquele país) aprovou o medicamento BRAFTOVI ® (encorafenib) em combinação com o
cetuximabe (comercializado
como ERBITUX ®), para o tratamento de pacientes adultos com câncer colorretal metastático
portadores da mutação BRAF
V600E, já tratados com terapias prévias.
Estudo mostra viabilidade de detecção precoce do câncer com exame de
sangue
 Detecção de câncer por exame de sangue poderia significar mais qualidade de vida e celeridade no
tratamento do paciente oncológico.
Detecção de câncer por exame de sangue poderia significar mais qualidade de vida e celeridade no
tratamento do paciente oncológico.
Foram coletados até 80 ml de sangue de cada um dos 15 254 participantes da América do Norte;
Estudos subsequentes comprovarão a aplicação clínica da tecnologia
Imagine poder diagnosticar o câncer precocemente por meio de uma simples coleta de sangue...A
realização dessa
possibilidade seria um grande avanço para a oncologia resultando em celeridade para o
tratamento, em mais qualidade de
vida e num processo menos dolorido e penoso para o paciente oncológico.
A boa notícia é que isso já está em andamento para se tornar realidade. Pesquisadores desenvolveram
o primeiro exame de
sangue que pode detectar com precisão mais de 50 tipos de câncer e identificar em qual
tecido o câncer se originou -
geralmente antes de haver sinais ou sintomas clínicos da doença.
Quarentena: uma oportunidade para repensar hábitos de
vida
 Com hábitos de vida saudáveis garantimos que o corpo poderá combater novas ameaças com toda
capacidade
Com hábitos de vida saudáveis garantimos que o corpo poderá combater novas ameaças com toda
capacidade
Ao contrário do coronavírus, que, além da higiene, exige cuidados extremos como isolamento
social, a prevenção contra o câncer inclui práticas que só trazem benefícios
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Em meio a uma pandemia sem precedentes no século 21, percebemos que várias das nossas
urgências, na verdade, podiam
esperar: fazer aquele tratamento de beleza, ir ao shopping, aproveitar a promoção, viajar no fim de
semana. A nossa
saúde, no entanto, não é uma dessas ‘coisas’ adiáveis. Afinal, o risco iminente de contágio
por coronavírus e
desenvolvimento da Covid-19 deixou claro: a saúde e a vida são nossos maiores
bens.
Pacientes oncológicos não devem interromper tratamentos e precisam
redobrar atenção contra Coronavírus

Pessoas em tratamento com quimioterapia, radioterapia, corticoterapia (corticoides),
imunossupressores, pacientes
hematológicos ou que foram submetidos a transplante de medula óssea têm o sistema imunológico
mais
debilitado
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Mesmo diante do alto poder de contágio por Coronavírus – COVID-19 e da confirmação de casos
em Belo Horizonte, algumas
pessoas ainda não entenderam a necessidade de seguir expressamente as recomendações de
prevenção. Com isso, colocam em
risco não só a própria família e amigos, mas toda a população.
Recomendações sobre Coronavírus para pacientes
oncológicos
 Além de seguir as recomendações de higiene, pacientes devem cuidar da alimentação
Além de seguir as recomendações de higiene, pacientes devem cuidar da alimentação
Tratamentos contra o câncer, como químio e radioterapia, podem enfraquecer o sistema imunológico
do corpo; pacientes devem redobrar a prevenção contra COVID-19
Pessoas com doenças cardiovasculares, no aparelho digestivo ou respiratório e em tratamento contra o
câncer ficam com o
sistema imunológico mais debilitado e, por isso, são consideradas mais propícias a contrair o
Coronavírus e desenvolver
a doença.
Tratamento da Helicobacter pylori em pessoas com história familiar de
câncer gástrico pode reduzir risco de desenvolver a doença
 Todos os casos de câncer gástrico foram detectados por meio das endoscopias de vigilância e quase
todos os casos (90,9%) eram de doença em estágio 1.
Todos os casos de câncer gástrico foram detectados por meio das endoscopias de vigilância e quase
todos os casos (90,9%) eram de doença em estágio 1.
Dados aumentam as evidências para a adoção de um programa de busca e erradicação da infecção em
países com alto risco de câncer gástrico
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
O que as bactérias do seu estômago têm a ver com o aparecimento de doenças sérias como câncer? Tudo!
A bactéria
Helicobacter pylori, por exemplo, está associada ao desenvolvimento de gastrite, úlcera péptica e
câncer gástrico em
todo o mundo. Recentemente, um estudo divulgado na revista Lancet Glob Health demonstrou que somente
essa bactéria foi
responsável 810.000 novos casos de câncer em 2018.
Utilidades da biópsia líquida além do câncer de pulmão
 Tumores sólidos como pulmão, mama, colorretal, melanoma, glândulas salivares, pâncreas e ovário
estão sendo analisados geneticamente com a tecnologia PCR Digital em Gotas
Tumores sólidos como pulmão, mama, colorretal, melanoma, glândulas salivares, pâncreas e ovário
estão sendo analisados geneticamente com a tecnologia PCR Digital em Gotas
Trabalho identificou, por meio de exames de sangue, alterações em genes de vários tumores sólidos
como pulmão
(células não pequenas - CPCNP), mama, colorretal, melanoma, glândulas salivares, pâncreas e
ovário
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Durante os mais de 30 anos em que sou oncologista, sempre me dediquei ao atendimento clínico e, ao
mesmo tempo, à vida
acadêmica e à pesquisa. Isso porque acreditava e acredito que devemos estar sempre em busca de
melhores ferramentas e
novos métodos científicos para a prevenção, diagnóstico e tratamentos do câncer.
5% DOS NOVOS CASOS ANUAIS DE CÂNCER NO MUNDO ESTÃO RELACIONADOS AO
CONSUMO FREQUENTE DE BEBIDAS ALCOÓLICAS
 Consumo diário de uma taça e meia de vinho (177ml), uma lata e meia de cerveja (500ml) ou menos
de um copo de uísque
(35ml) durante 10 anos aumenta o risco de câncer em 5%
Consumo diário de uma taça e meia de vinho (177ml), uma lata e meia de cerveja (500ml) ou menos
de um copo de uísque
(35ml) durante 10 anos aumenta o risco de câncer em 5%
Até 5% dos novos casos anuais de câncer no mundo estão relacionados ao consumo frequente de bebidas alcoólicas,
conforme
mostram dados da Sociedade
Americana de Oncologia Clínica. Um estudo publicado na revista Cancer é ainda mais
alarmante:
o consumo diário de uma taça e meia de vinho (177ml), uma lata e meia de cerveja (500ml) ou menos de
um copo de uísque
(35ml) durante 10 anos aumenta o risco de câncer em 5%. Após 40 anos, o risco de desenvolver a
doença aumenta em 54%.
Para o oncologista e oncogeneticista Dr. André Márcio Murad, trata-se de um dado alarmante, que
infelizmente não está
sendo levado à sério pela população: “As pessoas estão bebendo mais e bebendo bebidas mais pesadas.
Vemos que esse
hábito está sendo adotado inclusive pela população feminina. É assustador, pois isso o etilismo –
juntamente com outros
hábitos nocivos como o tabagismo, sedentarismo e obesidade – está diretamente relacionado ao aumento
da incidência e
mortalidade por diferentes tipos de cânceres como boca, faringe, laringe, esôfago, estômago, fígado,
intestino (cólon e
reto) e mama.”, alerta o médico.
CÂNCER DE INTESTINO PASSA A OCUPAR SEGUNDO LUGAR EM INCIDÊNCIA ENTRE
HOMENS BRASILEIROS
 Alimentação pouco saudável, rica em gordura e proteína animal, aumenta risco de desenvolvimento
do câncer
Alimentação pouco saudável, rica em gordura e proteína animal, aumenta risco de desenvolvimento
do câncer
Mudança é preocupante e demonstra, principalmente, maus hábitos de vida da população
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia
de Precisão e Personalizada
O Instituto Nacional do Câncer José de Alencar – INCA liberou recentemente as estatísticas de
incidência do câncer no
país, o que nos permite analisar o sucesso das ações preventivas. Infelizmente, os
números não são positivos e
demonstram a necessidade de atenção, tanto da população, quanto do Governo.
ADVOGADOS MINEIROS TÊM DESCONTO NA PERSONAL ONCOLOGIA DE PRECISÃO E
PERSONALIZADA
 Advogados terão acesso ao que há de mais moderno na Oncologia de Precisão e também ao pioneiro
Programa de Check-up Oncológico Personalizado
Advogados terão acesso ao que há de mais moderno na Oncologia de Precisão e também ao pioneiro
Programa de Check-up Oncológico Personalizado
Convênio firmado com a Caixa de Assistência dos Advogados – OAB MG confere benefícios nas
especialidades clínicas,
oncológicas, ultrassonografias, colonoscopias e em pequenos procedimentos
A Personal Oncologia renovou o atendimento aos advogados mineiros por meio do convênio com a Caixa
de Assistência dos
Advogados – OAB MG. Os advogados credenciados na OAB Convênios receberão descontos vantajosos para
usufruírem do
atendimento multidisciplinar e integrativo, incluindo especialidades clínicas, oncológicas,
ultrassonografias,
colonoscopias e em pequenos procedimentos.
DOENÇAS INFECCIOSAS ESTÃO ASSOCIADAS A 13% DOS CASOS DE CÂNCER NO
MUNDO
 Somente a Helicobacter pylori foi responsável por 810.000 novos casos de câncer em
2018
Somente a Helicobacter pylori foi responsável por 810.000 novos casos de câncer em
2018
Agentes bacterianos, como a Helicobacter pylori, e virais, como HPV, hepatite B e C foram
identificados como causas do surgimento de tumores
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia de
Precisão e Personalizada
Uma das angústias mais comuns entre pacientes oncológicos é não saber exatamente o porquê da doença
se desenvolver em
seu organismo. Como não conseguem relacionar a uma causa direta, muitas vezes, acreditam ser algum
tipo de castigo ou
provação. Outros, acham que foi devido a mágoas guardadas. A ciência, contudo, vem encontrando
respostas mais objetivas
como a exposição a fatores de riscos específicos.
CONFORTO PARA O PACIENTE ONCOLÓGICO
 Profissionais de enfermagem compõem equipe do setor de Procedimentos Propedêuticos
Profissionais de enfermagem compõem equipe do setor de Procedimentos Propedêuticos
Pequenos procedimentos e exames por imagem podem ser realizados na Personal Oncologia de Precisão
e Personalizada
Com uma equipe multidisciplinar e integrativa de ponta, a Personal Oncologia de Precisão e
Personalizada, por meio da
Personal Procedimentos Propedêuticos, está preparada para realizar uma grande variedade de
pequenos procedimentos
ambulatoriais, como biópsias e retiradas de lesão, e também exames por imagem como
ultrassonografias.
Imunoterapia administrada no tratamento da apresentadora Ana Maria
Braga utiliza tecnologia que ensina linfócitos T a matar células cancerígenas
 Ana Maria Braga anunciou um novo tratamento contra câncer de pulmão
Ana Maria Braga anunciou um novo tratamento contra câncer de pulmão
A apresentadora global Ana Maria Braga anunciou na segunda-feira (27), durante o programa Mais Você,
que está em
tratamento de um novo tumor no pulmão, dessa vez, uma adenocarcinoma
Conforme explica o oncologista e oncogeneticista Dr. André Márcio Murad, diretor Executivo da
Clínica Personal
Oncologia, existem quatros subtipos principais de câncer de pulmão: o adenocarcinoma que é
mais comum, o de células
escamosas, o de pequenas células e, menos frequentemente, o de células
grandes.
Queda da mortalidade por câncer nos EUA: importância da oncologia de
precisão
 Hábitos de vida pouco saudáveis são entrave para redução ainda maior da mortalidade por
câncer
Hábitos de vida pouco saudáveis são entrave para redução ainda maior da mortalidade por
câncer
Redução de 29% ocorreu entre 1991 e 2017, principalmente, para melanoma, tumores de pulmão, mama,
colorretal e
próstata, como mostra um novo relatório da American Cancer Society
Por
Dr. André Marcio Murad - Oncologista, oncogeneticista e diretor Executivo da Personal
Oncologia de Precisão e Personalizada
Muito se fala do nocivo modo de vida americano com fast-food em excesso, obesidade e
sedentarismo. Esses “hábitos” são
responsáveis pela desenvolvimento de inúmeras doenças, entre elas tipos de tumores
variados. Por isso, é surpreendente
quando descobrimos que a mortalidade por câncer no país caiu 29%, entre 1991 e 2017,
como mostra um novo relatório da
American Cancer Society.
Avanço na oncologia de precisão: tratamento alvo-molecular
direcionado à mutação KRASG12C
 Um novo inibidor da mutação KRASG12C foi avaliado para tratamento do câncer de pulmão de
células não pequenas
Um novo inibidor da mutação KRASG12C foi avaliado para tratamento do câncer de pulmão de
células não pequenas
Por
Dr. André Marcio Murad
Um ensaio de fase I sobre segurança, tolerabilidade, farmacocinética e eficácia do AMG 510 foi
considerado pioneiro e um
dos estudos mais importantes de 2019. Seu autor principal é Ramaswamy Govindan, da Escola de
Medicina da Washington
University, em St. Louis, nos EUA.
O fármaco, um novo inibidor do KRASG12C avaliado para tratamento do câncer de pulmão de
células não pequenas (NSCLC),
foi apresentado com muito entusiasmo na Conferência Mundial sobre Câncer de Pulmão 2019, organizada
pela International
Association for the Study of Lung Cancer (IASLC), em Barcelona, na Espanha..
Uso da análise de metilação em Oncologia
 Profissionais de enfermagem compõem equipe do setor de Procedimentos Propedêuticos
Profissionais de enfermagem compõem equipe do setor de Procedimentos Propedêuticos
Por Dr. André Marcio Murad*
As abordagens mais comuns para a detecção da metilação são baseadas na conversão de bases de
citosina não metilada em
uracila após o tratamento com bissulfito de sódio, que é então convertido em timidina durante a PCR.
Por esta abordagem,
os alelos metilados tratados com bissulfito têm diferentes sequências de DNA em comparação com os
correspondentes alelos
não metilados.
As diferenças entre as sequências de DNA metiladas e não metiladas podem ser avaliadas por vários
métodos, incluindo
análise de enzimas de restrição sensíveis à metilação, PCR específica para metilação, PCR
semiquantitativo,
sequenciamento Sanger, pirosequenciamento e sequenciamento de próxima geração.
SEGUNDO ESTUDO RECENTE, USO DE TINTURAS E ALISADORES ESTÁ ASSOCIADO A
UM RISCO MAIOR DE APARECIMENTO DO CÂNCER DE MAMA EM MULHERES
 Produtos utilizados para tintura e alisamento podem conter mais de 5000 substâncias
químicas
Produtos utilizados para tintura e alisamento podem conter mais de 5000 substâncias
químicas
Produtos utilizados para ambos procedimentos estéticos podem conter mais de 5000 substâncias
químicas, incluindo
algumas com propriedades mutagênicas e desreguladoras do sistema endócrino
*Dr. André Murad – Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia
de Precisão e Personalizada
Mudar a cor do cabelo parece ser hoje uma necessidade que vai além do objetivo de esconder os
fios brancos, como era há
algumas décadas. É um requisito de beleza para mulheres, homens e adolescentes. O chamado
alisamento também é muito
utilizado, apesar de nos últimos anos ter perdido espaço diante da valorização do cabelo mais
natural.
Conheça os alimentos que devem ser acrescidos e os que devem ficar
fora de uma dieta preventiva do câncer
 Erros alimentares levam ao consumo de substâncias cancerígenas
Erros alimentares levam ao consumo de substâncias cancerígenas
Pesquisas demonstram que os erros alimentares e o consumo exagerado de substâncias potencialmente
cancerígenas podem ser
responsáveis por cerca de 40% dos casos dos cânceres existentes.
Uma dieta rica em calorias, gordura saturada e proteína animal e pobre em fibra vegetal é
relacionada ao surgimento
de tumores de mama, endométrio, próstata, intestino grosso e vesícula biliar.
Carnes artificialmente conservadas, especialmente as salgadas e defumadas, como a carne de
sol e o bacon causam
câncer de estômago e esôfago.
Entenda o que é e quais são as causas do câncer
 O câncer não é uma doença contagiosa
O câncer não é uma doença contagiosa
Câncer é uma doença causada por alterações no DNA das células as quais resultam em um uma
divisão de maneira
descontrolada das mesmas. Estas células duplicam-se de forma muito rápida e, após algum
tempo, podem invadir outras
partes do corpo.
Causas
O câncer é causado, na maioria das vezes, por fatores ambientais (70%) e genéticos (15%). Ou
seja, o câncer não é uma
doença contagiosa e não passa de uma pessoa para outra.
FDA aprova olaparibe como tratamento de manutenção para câncer
pancreático metastático com mutação no BRCA
 O órgão regulador americano baseou sua aprovação nos resultados do estudo POLO randomizado de
fase 3
O órgão regulador americano baseou sua aprovação nos resultados do estudo POLO randomizado de
fase 3
O FDA aprovou o olaparibe como tratamento de manutenção para adultos com câncer pancreático
metastático deletério ou
suspeito de sofrer alterações no BRCA, de acordo com um comunicado de imprensa do fabricante do
medicamento. A aprovação
do olaparibe (Lynparza; AstraZeneca, Merck) se aplica a pacientes cuja doença não
progrediu após pelo menos 16 semanas
de quimioterapia de primeira linha com platina.
"Pacientes com câncer de pâncreas avançado historicamente enfrentam maus resultados devido à
natureza agressiva da
doença e avanços limitados no tratamento nas últimas décadas", disse Dave Fredrickson,
vice-presidente executivo e chefe
da unidade de negócios de oncologia da AstraZeneca, no comunicado. "[Olaparib] agora é o único
medicamento direcionado
aprovado para pacientes selecionados com biomarcadores com câncer pancreático avançado".
Diagnóstico precoce aumenta as chances de cura do câncer de
intestino
 Prevenção e rastreamento devem ser personalizados conforme riscos a cada pessoa está exposta
Prevenção e rastreamento devem ser personalizados conforme riscos a cada pessoa está exposta
Infelizmente, tanto a prevenção quanto o rastreamento da doença são negligenciados pela população
causando aumento de
sua incidência e mortalidade
Dr. André Murad - Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia
de Precisão e Personalizada
Uma paciente portadora de câncer de intestino grosso já avançado, com
metástases no fígado e pulmões, me procurou há
cerca de dois anos, pois havia sido tratada, sem sucesso, com uma combinação de quimioterapia e
cetuximabe – um
anticorpo monoclonal que ataca células que expressam o fator de crescimento epitelial.
Embora raro, câncer cerebral apresenta baixas taxas de cura e
sobrevida
 Marie Fredriksson, vocalista da famosa dupla sueca Roxette faleceu de câncer no cérebro após 17
anos lutando contra a doença
Marie Fredriksson, vocalista da famosa dupla sueca Roxette faleceu de câncer no cérebro após 17
anos lutando contra a doença
Os sintomas da doença variam conforme localização do tumor no cérebro e incluem dores de cabeça,
convulsões,
problemas de visão, vômitos, déficits motores e sensoriais, perturbações mentais e dificuldade
de caminhar e falar
Dr. André Murad - Oncologista, oncogeneticista e diretor Executivo da Personal Oncologia
de Precisão e Personalizada
Volta e meia alguma personalidade vira notícia ao ser diagnosticada com algum tumor, a exemplo do
atual prefeito de São
Paulo, Bruno Covas, que se trata de um câncer na cárdia - transição entre o esôfago e o estômago -
com metástase no
fígado; ou ao falecer devido o avanço do tumor, como Marie Fredriksson, vocalista da famosa dupla
sueca Roxette.
Profissionais Personal Oncologia passam por treinamento de
atualização sobre Primeiros Socorros
 cardiologista Dr. Fabrício Pelucci atualizou os conhecimentos da equipe sobre procedimentos de
Ressuscitação Cardiopulmonar - RCP
cardiologista Dr. Fabrício Pelucci atualizou os conhecimentos da equipe sobre procedimentos de
Ressuscitação Cardiopulmonar - RCP
Enfermeiros, biomédicos, farmacêuticos e demais profissionais que compõem as equipes de Pesquisa
Clínica e de Enfermagem da Personal Oncologia de Precisão e Personalizada participaram da
atualização
Na segunda-feira, 16, o cardiologista Dr. Fabrício Pelucci conduziu o treinamento sobre manobras de
primeiros socorros em casos de parada cardiorrespiratória, para parte da equipe Personal Oncologia.
O objetivo foi atualizar o conhecimento dos profissionais em caso de urgências e emergências.
“Toda a equipe, até mesmo a recepção, deve estar preparada para alguma situação adversa.
Principalmente por estarmos em
uma clínica, temos que nos preocupar com a segurança do paciente. Então, a equipe estando sempre
capacitada e
atualizada, estamos prontos para lidar com situações adversas”, detalha a Coordenadora de enfermagem
e RT, Bruna
Azevedo.
Entenda por que o exame oncológico preventivo é decisivo para cura de
câncer

Brasil tem 600 mil casos novos de câncer ao ano, dos quais 15%, hereditários. Diagnóstico precoce
pode, portanto, salvar 90 mil pessoas anualmente
Dr. André Murad
Oncologista e oncogeneticista
Há pouco mais de dois anos, tive um paciente relativamente jovem, com cerca de 51 anos,
diagnosticado e tratado de um
sarcoma (tumor na musculatura da coxa). Um ano depois, detectei um novo tumor, um câncer
de próstata. Devido ao
histórico familiar dele, com vários tipos de câncer em pessoas abaixo dos 55 anos, suspeitei da
Síndrome de Li-Fraumeni
(LFS), que é causada pela mutação do gene TP53
Seus hábitos de vida causam ou previnem o câncer?
 Hábitos de vida saudáveis são fundamentais para manter uma boa saúde (foto:
Pixabay/reprodução)
Hábitos de vida saudáveis são fundamentais para manter uma boa saúde (foto:
Pixabay/reprodução)
Obesidade está aumentando em todo o mundo e com ela a mortalidade por uma série de doenças,
incluindo o câncer
Dr. André Murad
Oncologista e oncogeneticista
Quem teve o privilégio de crescer até a década de 80 e 90, especialmente, em cidades do interior,
deve se lembrar bem de
como a vida nos exigia muito mais esforço físico do que hoje. Os elevadores e as escadas rolantes
não faziam parte da
nossa rotina. Para mudar o canal da TV e a frequência do rádio, tínhamos que levantar e caminhar. Ir
à padaria, ao
armazém... tudo isso fazíamos a pé.
Autocuidado é fundamental na luta contra o câncer
 Hoje, é possível sequenciar praticamente o genoma inteiro em questão de horas e com o custo muito
mais baixo.
Hoje, é possível sequenciar praticamente o genoma inteiro em questão de horas e com o custo muito
mais baixo.
Como 15% dos cânceres são determinados por fatores genéticos, no caso das mulheres essa
informação é usada para rastrear a doença
Dr. André Murad
Oncologista e oncogeneticista
A genética molecular na oncologia é um verdadeiro paradigma que fez a área dar um salto em evolução
(foto: HCOR/reprodução)
Ao analisar o caso de uma paciente com câncer de mama, um tempo atrás, deparei-me com a constatação
do quanto o
entendimento do genoma humano foi um divisor de águas para a oncologia. O quadro dela
é interessante por diferentes
fatores e nos mostra a importância do autocuidado e do rastreamento do tumor.
Precisamos falar sobre câncer
O papel da população na luta contra o câncer é justamente desmistificar, informar-se
corretamente, fazer prevenção e buscar o diagnóstico precoce
Dr. André Murad
Sou oncologista há 30 anos e, mesmo depois de tanto tempo, ainda percebo o tabu existente em cima da
palavra “câncer”.
Infelizmente, a consequência direta disso é a dificuldade da população em buscar o diagnóstico
precoce, o que impacta
diretamente no crescimento da incidência e da mortalidade. Para expor esse meu ponto de vista, peço
ao leitor que faça a
análise: o que vem à sua mente quando pensa nesse termo?
Estudo mostra custo-efetividade de testes genéticos com painéis
multigênicos para todas as pacientes com diagnóstico de câncer de mama
 Testes dos genes BRCA1, BRCA2 e PALB2 em todas as pacientes com câncer de mama poderia se
traduzir em 2.101 casos a menos de câncer de mama ou ovário em um ano.
Testes dos genes BRCA1, BRCA2 e PALB2 em todas as pacientes com câncer de mama poderia se
traduzir em 2.101 casos a menos de câncer de mama ou ovário em um ano.
Este estudo de modelagem de micro-simulação de custo-benefício comparou os custos e os efeitos no
tempo de vida dos
testes de alto risco (multigênicos) de todos os pacientes com câncer de mama não selecionados
(estratégia A) com o teste
BRCA1/BRCA2 com base no histórico familiar ou critérios clínicos (estratégia B) em populações do
Reino Unido e Estados
Unidos.
Com base nos dados de 11.836 pacientes com câncer de mama no Reino Unido, EUA e Austrália que foram
testados para
variantes de alto risco nos genes BRCA1, BRCA2 e PALB2 - juntamente com informações sobre
estratégias de triagem e
intervenções relacionadas para aqueles com variantes relacionadas ao câncer nesses genes - os
pesquisadores concluíram
que a abordagem não selecionada era rentável para as fontes pagadoras e para a sociedade em cerca de
98 a 99% das
simulações do sistema de saúde do Reino Unido e entre 64 e 68% das simulações feitas no contexto do
sistema de saúde dos
EUA.